掲載日:2019年5月
白血病とは
-
-
「白血病」というと、「血液のがん」と想像される方も多いのではないでしょうか。実は血液の病気では悪性リンパ腫のほうが圧倒的に多いのですが、なぜか白血病のほうが有名です。白血病は子供のがんの中では一番多いです。
そして、20代から40代までの人はなんと病気による死亡原因の1位なのです。ついこの間まで元気であった若い人が突然命にかかわる病気になる。本人も周りの人もこれほどびっくりすることはありません。そのため印象深いのだと思います。
白血病は遺伝子変異の蓄積でおこる!
「どうして白血病になんかなってしまったのですか?子供にはうつるんですか?」と患者さんのご家族からよく聞かれます。白血病を含めた悪性腫瘍は遺伝子変異の蓄積によって起こります。通常、胃がんや肺がんなどの固形ガンでは100種類くらいの遺伝子異常が見られるのに対し、急性骨髄性白血病では平均13種類程度の遺伝子変異が見られます(図①)。
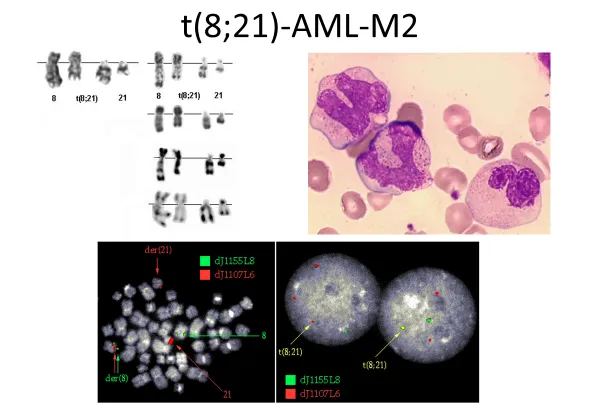
このような遺伝子変異は子供にはうつりません。急性骨髄性白血病200サンプルのいずれかで認められた遺伝子変異の総数は約1,600種類におよび、反復性変異のなかでの高頻度変異として12種の遺伝子変異が同定されました(図②)。
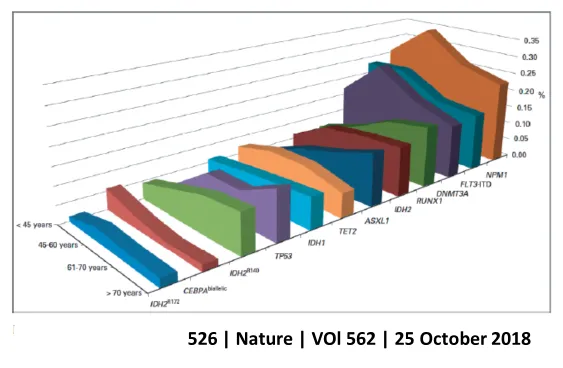
遺伝子変異はその機能 などに基づいて、①転写因子融合 18%(PML-RARA,MYH11-CBFB,RUNX1-RUNX1T1など)、 ②NPM1遺伝子 27%、③がん抑制遺伝子 16%(TP53,WT1など)、④DNAメチル化関連 44% (DNMT3A,TET2,IDH1/2など)、⑤シグナル伝達5 9%(FLT3,KITなど)、⑥骨髄球系転写因子 22%(RUNX1,CEBPAなど)、⑦クロマチン修飾 30%(MLL-PTD,ASXL1,EZH2など)、⑧コヒーシン 13%、⑨スプライソゾーム 14%、の9種類に分類されます。これらの遺伝子変異群は協調的または排他的にはたらくことで急性骨髄性白血病の発症に関与することが明らかにされています。そのなかでも、FLT3、 NPM1、DNMT3Aは全ての患者さんの20%以上の頻度で遺伝子変異が認められ、高頻度に他の遺伝子変異と重複して存在しており、複数の遺伝子変異と協調して急性骨髄性白血病発症にはたらくと考えられます。
年齢とともに遺伝子変異の蓄積は誰にも平等におこる!
最近では、90歳以上の御高齢の方も多く見うけられるようになりましたが、ヒトは年齢が嵩むにつれ、体の細胞に遺伝子異常を持った細胞が増加します。海外の研究発表では60歳代になると遺伝子異常を持った細胞は急激に増加し、CHIP (Clonal Hematopoiesis Indetermined Signature)と呼ばれる一群の細胞が増えることが報告されています(図③)。特に、DNMT3A、 ASLX-1、TETの遺伝子変異を持つヒトは白血病を含めた造血器腫瘍の発症頻度が40倍くらいに増加することが知られています。さらに、EZH2変異を持つヒトは生活習慣病が原因と目されている心筋梗塞の発症頻度が増加することも知られています。つまり、ガンが発病するのは生きていく上での宿命であり、この遺伝子の交通事故は誰でも平等に出会うわけであります。まず、CHIPがおこり、前がん状態になった細胞にDriver mutation (病気を積極的に発病させる遺伝子変異)が乗っかると白血病が出来上がります。
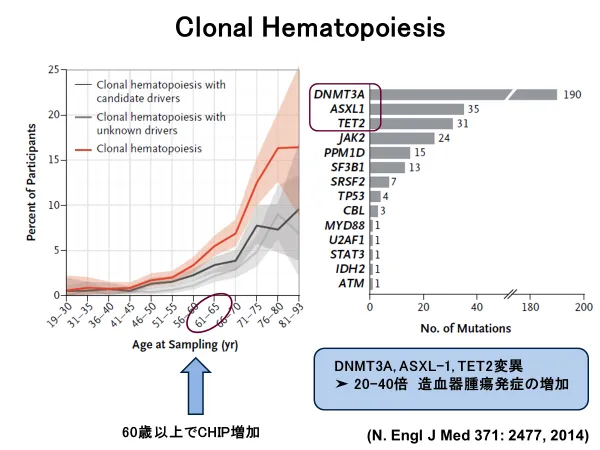
難しくいうと急性骨髄性白血病の発症は、まず造血幹細胞レベルにおいてクラスII遺伝子変異(PML-RARA,RUNX1-RUNX1T1など)やNPM1またはエピゲノムに関与する遺伝子変異(DNMT3A,IDH2,TET2など)がinitiating変異として生じてinitiatingクローン、すなわち前白血病クローンとなります。さらにFLT3やRASなど細胞増殖に関与するdriver変異を獲得して、クローンサイズを拡大させ、foundingクローンとなり、さらに複数のpassenger変異が加わり、急性骨髄性白血病は初診時から複数のサブクローンで構成されると考えられます。また、急性骨髄性白血病においてDNMT3AとIDH2変異について詳細な検討を行った研究では、DNMT3A変異は白血病芽球のみならず、低頻度ながら正常造血前駆細胞および T細胞にも検出され、さらに寛解期にもDNMT3A変異陽性の幹細胞が存在し、再発に寄与するクローンサイズを拡大させることが知られています。このように前白血病クローン成立にも、重複する遺伝子変異の順番が存在すると考えられます。
日本の白血病治療は米国の5年遅れである!
私はこれまで毎年、米国血液学会に出席し自分の研究結果を講演発表、ポスター発表を行ってまいりました(図④)。

その中で感じたのは、日本における白血病治療は米国の5年遅れであるという真実です。なんでこんなにも遅れてしまったのか? 原因は社会基盤に起因するところが非常に大きいと思います。米国では国、民間企業、患者団体、病院、臨床医、研究医が一体となって遂行されている一大事業、Beat AMLというプロジェクトがあります。これは各団体の垣根を越えて「すべては患者さんのために」という発想であり患者検体から得られた情報により新規薬剤開発が非常にスムースにゆく試みです(図⑤)。
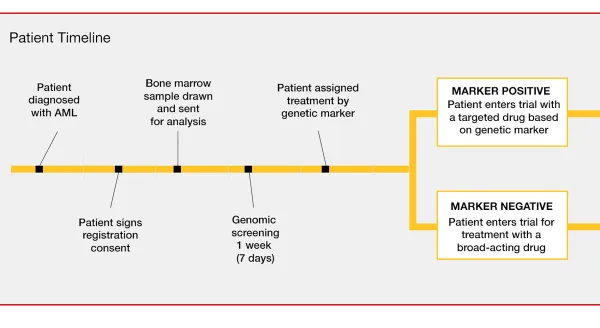
一人の白血病患者が病院を受診すると、その患者さんはBeat AMLプロジェクトに参加するかどうかを病院の治験管理室の担当者より説明を受け、同意された場合に患者さんの白血病細胞は遺伝子検査をする研究所に送られます。2週間程度で得られた遺伝子解析の結果より、その白血病細胞に一番効果のある分子標的薬剤が選び出され(図⑥)、臨床試験として患者さんに投与され、試験管の上のデータが実臨床の成績に反映されるかを解析します。

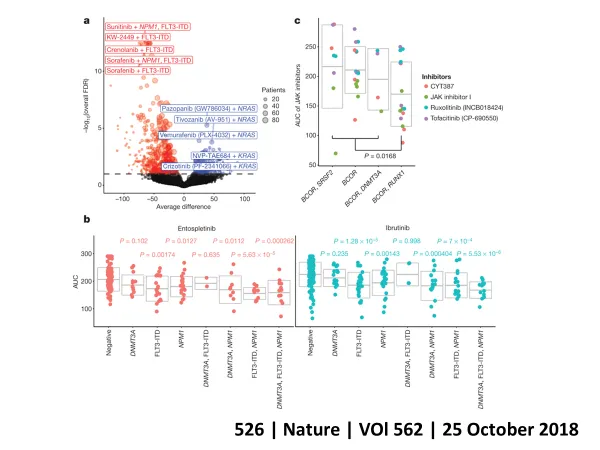
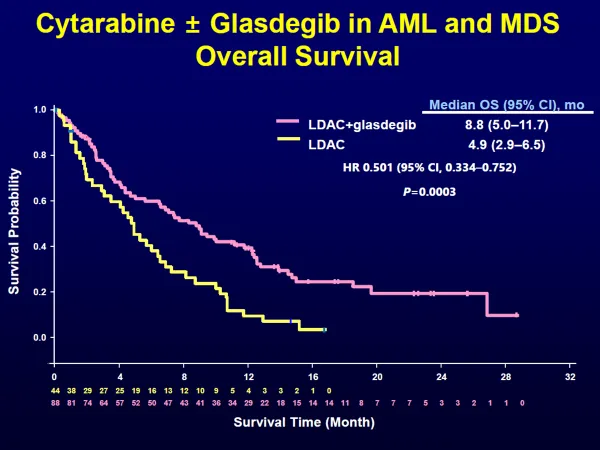
もし、試験薬剤が非常に効果的であれば米国FDAは副作用等の臨床試験成績を監査し、新規薬剤の承認を与える流れになるため短期間で新規治療法が確立します。驚くことに、この米国のプロジェクトには日本企業である武田製薬、アステラス製薬も参加しているという事実です。日本で現在、行われているのは遺伝子解析までであり、その先がなかなか繋がりません。これが、「日本の白血病治療は米国の5年遅れである」という根拠です。このような状況の中で、私共の前臨床試験の結果から得られた情報をもとに国際臨床試験が構築され、造血幹細胞移植が適応とならない急性骨髄性白血病症例の全生存期間を2倍に延長することに成功いたしました(図⑦)。
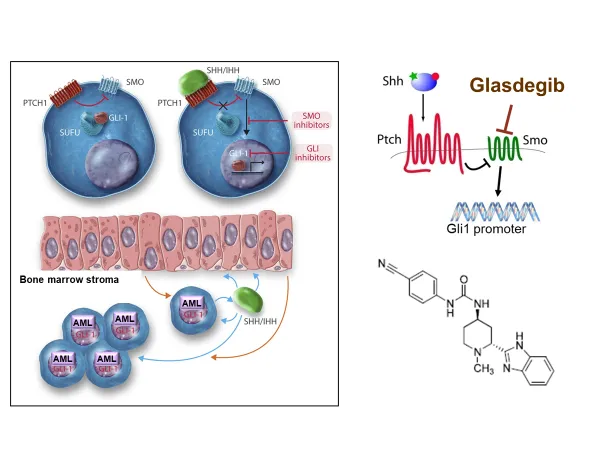
すべては患者さんのために!
日本における社会基盤の革新はなかなか進まないのが事実としてあります。この状況の中で各医療人が病気で苦しんでおられる患者さんのために何かしてあげようとする気持ちが社会基盤の革新に繋がるのではないでしょうか。
